항생제 내성
진화가 작동 중인가?
Don Batten 글, 이종헌 역
출처: creation magazine Vol. 39(2017), No. 4 pp. 46-48

항생제의 발견은 의학에서 가장 중요한 진보 중 하나였으며 인간의 건강을 근본적으로 향상 시켰다. 종종 사람들을 죽인 많은 세균 감염(예를 들면, 결핵 및 상처 감염)이 치료 가능 해지고 수백만 명의 목숨을 살렸다.
예를 들면, 1930년대에 도입된 지 15 여년이 지났을 때, 미국에서의 사망자 수는 1년에 인구 10만 명당 약 220명이 감소했다. 다른 모든 의료 기술은 향후 45년 동안 사망자수를 추가로 약 20명 정도 줄였을 뿐이다.[1]
그러나 항생제에 대한 내성의 발달은 이러한 성공을 위협한다. 전 세계적으로 현재 사용 가능한 항생제의 많은 또는 모든 것에 박테리아 내성에 의한 감염이 증가하고 있다. 더욱이, 새로운 항생제를 개발하는 회사는 점점 줄어들고 있다. 1990년에는 18개 회사가 있었지만 2011년에는 4개 회사 밖에 없었다.[2] 이러한 감소의 주된 이유는 새로운 항생제의 도입에 곧바로 뒤이어 내성이 생긴다는 것을 알게 되었고, 새로운 항생제를 개발하는 데 많은 비용이 든다는 것이다. 2015년에 발표된 새로운 종류의 항생제 발견은 1987년 이래 처음이다.[3]
학교와 대학에서 사용되는 생물학 교과서는 항생제 내성을 종종 ‘작동 중인 진화’의 예라고 제시하고 있다. 그래서 미생물이 수십억 년 동안에 미생물학자로 변할 수 있다는 것을 증명하는 것이라고 생각한다. 그러나 내성의 기초가 되는 생화학적 메커니즘에 대한 연구는 내성의 발달이 그러한 ‘큰 그림’의 진화적 변화에 아무런 도움이 되지 않는다는 것을 보여준다. 발견된 변화의 유형은 생명체에 대한 창조론자의 견해를 지지하며, 자연적 변화는 제한적이고, 하나의 기본적인 유기물이 다른 종류로 변화할 수 없다.
The mechanisms of resistance(내성의 메커니즘)
과학자들은 내성에 대해 세 가지 일반적인 범주를 발견했다.
1. 항생제 표적의 변경 또는 보호
2. 표적에 대한 약물 접근의 제한
3. 항생제의 비활성화.
1. Alteration or protection of the target(표적의 변경 또는 보호)
콜리스틴(폴리믹신 E라고도 함)이 그 한 예이다. 몸 안에서 콜리스틴은 특정 박테리아(그람 음성 박테리아)의 외막에 존재하는 음전하를 띤 분자(리포다당류 또는 LPS/lipopolysaccharide)에 부착하는 양전하를 띤 분자이다. 이 결합은 박테리아를 죽이는 과정에서 필수적인 첫번째 단계이다.
하나의 특정한 박테리아에서의 돌연변이는 리포다당류의 생성을 방해한다. 따라서 이것은 콜리스틴이 박테리아에 결합하여 박테리아를 죽이는 것을 방지한다.[4]
이 결합이 실패하는 것 역시 더 복잡한 메커니즘이 있다. 음전하를 띤 LPS에 결합하는 양전하를 띤 마그네슘 이온은 보통 이러한 유형의 박테리아의 세포막을 안정화시킨다. 마그네슘의 농도가 낮으면 박테리아는 음전하를 차단하여 막을 안정하게 유지하는 시스템을 갖추고 있다. 세포는 이 차단을 조절하는 제어 시스템을 가지고 있는데 필요할 때만 켠다. 돌연변이로 인해 제어 시스템이 손상되면 차단 시스템이 계속 켜질 수 있다. 세포는 그것을 끌 수가 없다. 노출된 음전하가 감소한다는 것은 여기서도 항생제가 세포에 결합하여 그것을 죽일 수 없다는 것을 의미한다. 이 경우 돌연변이 된 세포는 시스템이 필요하지 않을 때 자원을 낭비하므로 박테리아는 항생제가 없을 때 생존률이 떨어진다.
어떻든 여기서 봐야 할 것은, 관련된 돌연변이는 새로운 효소 또는 단백질과 관련된 새로운 메커니즘을 만들어 내는 것이 아니라 기존의 기능을 파괴한다는 것이다.
2. Restriction of the drug’s access to the target(표적에 대한 약물 접근의 제한)
많은 항생제들이 박테리아를 죽이기 위해서는 그 안으로 들어가야 한다. 한 예로 포스포마이신이 있는데, 그것은 세포벽의 결정적인 구성 요소를 만드는 것을 막음으로써 박테리아를 죽인다. 박테리아 세포벽에는 세포 내로 영양분을 이동시키는 다양한 수송 용 ‘펌프’가 있다. 이들 수송체는 그들이 수송하는 물질에 있어서 매우 선택적이지만, 포스포마이신은 구조적으로 그들이 섭취하는 일반적인 영양소 중 하나와 같아서 거기에 편승하여 세포 속으로 들어간다.
세포가 수송체를 만드는 방식을 특정하는 유전자 안에서 혹은 그것들의 생산을 자극하는 조절자 유전자 안에서 일어나는 돌연변이는 수송체를 생기지 않게 하거나 수송체가 덜 효과적이 되게 할 수 있다. 이것은 포스포마이신이 세포 안으로 아예 혹은 거의 들어가지 못한다는 것을 의미한다. 그러한 세포는 포스포마이신에 내성이 있다.
다시 한번, 돌연변이는 세포의 정상적인 기능을 파괴한다; 그것들은 새로운 유전자, 새로운 단백질 또는 효소를 생성하지 않는다. 내성 세포는 ‘새로운 개량 모델’과는 거리가 멀게, 이제는 수송체가 손상되었거나 없어서 보통은 수송체를 통해 들어가던 양의 식품 물질을 받아들일 수 없다. 따라서, 항생제가 없는 경우, 민감한 박테리아가 보통 내성 박테리아보다 우위에 있을 것이다; 그래서 내성 박테리아는 전체 박테리아 개체군의 작은 비율을 차지할 뿐이다.
Reverse pumps(가역 펌프)
많은 종의 박테리아는 독소와 같은 물질을 세포 밖으로 밀어내는, ‘유출 펌프’라고 불리는 펌프를 가지고 있다. 이들은 또한 항생제를 세포 밖으로 퍼내어 항생제가 세포를 죽이는 것을 멈추게 할 수 있다. 유출 펌프의 제조와 관련된 유전자의 조절은 복잡하지만, 펌프의 수를 제한하는 조절자의 돌연변이로 인해 더 많은 펌프가 만들어져 항생제에 대해 세포 내성이 생길 수 있다. 이런 방식의 내성은, 특히 저항 방식은 플루오로퀴놀론 계 항생제에 특히 중요하다.[5] 또한 조절하는 시스템이 깨지면 세포는 필요하지 않을 때에 과도하게 펌프를 만들면서 자원을 낭비하고 있다; 따라서 돌연변이된 세포는 항생제가 없을 때 생존하기에 덜 적합하다.
여기서 각각의 경우에서 있어서, 돌연변이는 펌프 자체 혹은 그것을 생산을 조절하는 시스템을 ‘파괴하는’ 유전자이다. 이것은 박테리아에서 세균학자로 진행하는 진화를 위해 필요한 새로운 유전자를 만드는 돌연변이를 지원하지 않는다.
3. Inactivation of the antibiotic(항생제의 비활성화)
박테리아에 의해 제조된 효소는 항생제를 분해(신진대사) 할 수 있다. 예를 들어, b-락타마제라고 불리는 효소는 페니실린을 분해 할 수 있다. 박테리아가 항생제를 만나서 그런 능력을 얻는 것은 새로운 효소, 즉 새로운 유전자가 생기는 진화의 훌륭한 예가 될 것처럼 보일 것이다. 그러나, 알려진 경우에 있어서, 항생제를 파괴하는 효소를 제조하는 기계가 돌연변이에 의해 발생하는 것이 관찰 된 적이 없다. 그러면 그것은 어떻게 생겨난 것일까?
Gene transfer(유전자 전달)
지금은 박테리아 세포가 항생제를 분해하는 능력을 얻는 것은 이미 내성을 갖는 다른 박테리아로부터라는 것이 알려져 있다.
그러한 내성을 위한 유전자는 단일 원형 박테리아 염색체의 외부에 있는 플라스미드(염색체와는 따로 증식할 수 있는 유전인자)라고 불리는 작은 DNA 고리(loops)에 존재할 수 있다. 이들 플라스미드는 다른 박테리아들 사이에, 심지어 다른 종 사이에서도 전달될 수 있다.[6] 하나의 민감한 수용자 메커니즘은 내성 플라스미드를 갖는 박테리아를 내성이 없는 박테리아와 튜브(섬모)를 통해 연결되도록 한다.[7] 내성 박테리아는 플라스미드를 복제하고 민감한 박테리아에게 사본을 ‘기부’한다(아래의 도표를 보라).
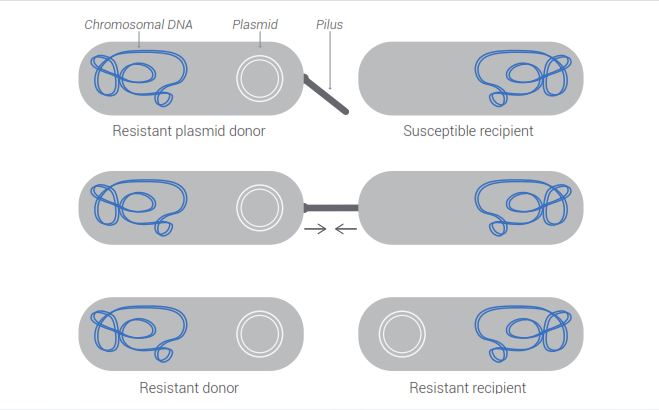
(염색체 DNA, 플라스미드, 섬모, 내성 플리스미드 기증자, 민감한 수용자. 내성 기증자, 내성 수용자)
많은 플라스미드는 항생제의 여러 종류에 대해 복합적으로 내성을 갖는 유전자를 가지고 있다. 다시 말하지만, 이런 종류의 내성에는 새로운 유전자가 들어 있는 것이 아니라, 기존의 유전자가 내성 유형에서 민감한 유형으로 전달되는 것이다.[8]
Breaking control systems(제어 시스템을 분해하기)
페니실린에 대한 내성은 고전적인 예를 제공한다. 일부 박테리아는 그들의 환경에서 자연적으로 발생하는 소량의 페니실린을 분해하기 위해 소량의 페니실리나제(페니실린 분해 효소)를 생성하지만 환자에게 투여되는 양에 대처할 만큼 충분하지는 않다. 생산된 페니실리나제의 양을 제한하는 시스템의 돌연변이는 훨씬 더 많은 분해효소가 만들어지는 것을 의미할 수 있어서, 박테리아가 내성을 가질 것이다. 그러나 위의 다른 사례와 마찬가지로, 자연상태에서는 이들 내성을 갖는 박테리아는 페니실리나제의 생성을 더 이상 제어할 수 없어서, 페니실리나제 생산에 희소한 자원을 낭비하지 않는 박테리아보다 우위에 있을 것이다.
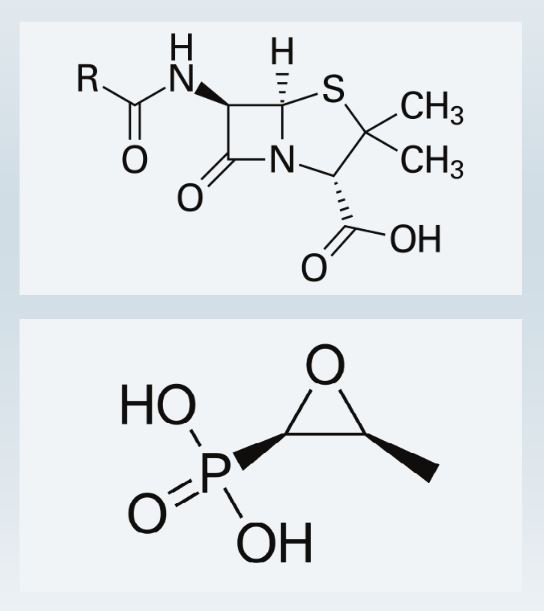
<두 가지 항생제의 화학적 구조: 페니실린(위)과 포스포마이신(아래)>
Natural selection?(자연선택?)
이 모든 경우에서 자연 선택은 많은 항생제가 있는 곳에 있는 내성 균주를 선호 할 것이다. 그러나 자연 선택은 내성의 생존을 설명하지만, 내성의 출현을 설명하지는 않는다. 내성은 기존 시스템을 수정(보통 분해하기)하거나 혹은 이미 그것을 가지고 있는 시스템에서 유전자를 전달함으로써 발생한다. 돌연변이가 무언가를 분해하면 자연 선택은 자연상태에서 내성 균주를 제거하는 경향이 있지만 항생제가 포화된 환경에서는 그들을 선호한다.
Conclusion(결론)
항생제 내성에 대한 연구 결과 박테리아가 항생제에 생존하기 위해 적응하는 것을 돕는 자연선택과 돌연변이의 몇가지 좋은 예가 드러났다. 그러나 그 어떤 발견도, 기존의 유전자/DNA에 대한 우연한 변화(돌연변이)가 미생물을 인류, 망고 및 밍크 고래로 전환시키는 데 필요한 수천 개의 새로운 유전자와 유전자 네트워크를 생성시킬 수 있다는 개념을 지지하지는 않는다. 사실상, 연구 된 변화는 ‘상향’ 진화의 측면에서 돌연변이가 얼마나 제한적인지를 강조할 뿐이다.
References and notes(참고문헌과 노트)
1. Spellberg, B., The antibacterial pipeline: why it is drying up, and what must be done about it, In: Antibiotic Resistance: Implications for Global Health and Novel Intervention Strategies: Workshop Summary, National Academies Press, p. 327, 2011.
2. Cooper, M.A. and Shlaes, D., Fix the antibiotics pipeline, Nature 472(7341):32, 2011 | doi:10.1038/472032a.
3. Ling, L.L. et al., A new antibiotic kills pathogens without detectable resistance, Nature 517(7535):455–459, 2015 |doi:10.1038/nature14098; the antibiotic is called teixobactin.
4. Moffatt, J.H. et al., Colistin resistance in Acinetobacter baumannii is mediated by complete loss of lipopolysaccharide production, Antimicrob. Agents Chemother. 54(12):4971–7, 2010 | doi: 10.1128/AAC.00834-10.
5. Blair, J.M.A., Richmond, G.E., and Piddock, L. J.V., Multidr ug efflux pumps in Gramnegative bacteria and their role in antibiotic resistance(review), Future Microbiology 9(10):1165–1177, 2014; | doi:10.2217/fmb.14.66.
6. There are other ways that resistance genes can be transferred as well, involving bacteriophages (a virus that infects bacteria), transposons, and ‘naked DNA’.
7. This is called ‘conjugation’.
8. Evolutionists assume that these genes (for example, to make the penicillin-destroying enzyme b-lactamase) must have originally arisen by mutation, but that belief is not what is observed.
DON BATTEN, B.Sc.Agr.(Hons.), Ph.D.
Dr Batten worked as a research scientist and consultant plant physiologist and is now the Managing Director of Creation Ministries International in Brisbane, Australia. For more: creation.com/batten.

 히브리어 교수가 창세기는 실제 역사임을 확증하다 - Jonathan Sa...
히브리어 교수가 창세기는 실제 역사임을 확증하다 - Jonathan Sa...
 하나님의 푸는 모터 국소이성화효소(topoisomerase) - Jonathan S...
하나님의 푸는 모터 국소이성화효소(topoisomerase) - Jonathan S...